Где происходит синтез атф
Содержание:
Энергетический обмен в клетке. Синтез АТФ.
Синтез АТФ происходит в клетках всех организмов в процессе фосфорилирования, т.е. присоединения неорганического фосфата к АДФ. Энергия для фосфорилирования АДФ образуется в ходе энергетического обмена. Энергетический обмен, или диссимиляция, представляет собой совокупность реакции расщепления органических веществ, сопровождающихся выделением энергии. В зависимости от среды обитания диссимиляция может протекать в два или три этапа.
У большинства живых организмов ― аэробов, живущих в кислородной среде, ― в ходе диссимиляции осуществляется три этапа: подготовительный, бескислородный, кислородный. У анаэробов, обитающих в среде лишенной кислорода, или у аэробов при его недостатке, диссимиляция протекает лишь в два первых этапа с образованием промежуточных органических соединений, еще богатых энергией.
Первый этап – подготовительный. В желудочно-кишечном тракте многоклеточных организмов он осуществляется пищеварительными ферментами. У одноклеточных – ферментами лизосом. На первом этапе происходит расщепление белков до аминокислот, жиров до глицерина и жирных кислот, полисахаридов до моносахаридов, нуклеиновых кислот до нуклеотидов. Этот процесс называется пищеварением.
Второй этап – бескислородный (гликолиз). Его биологический смысл заключается в начале постепенного расщепления и окисления глюкозы с накоплением энергии в виде 2 молекул АТФ. Гликолиз происходит в цитоплазме клеток. Он состоит из нескольких последовательных реакций превращения молекулы глюкозы в две молекулы пировиноградной кислоты (пирувата) и две молекулы АТФ, в виде которой запасается часть энергии, выделившейся при гликолизе:
Остальная энергия рассеивается в виде тепла.
В клетках дрожжей и растений (при недостатке кислорода) пируват распадается на этиловый спирт и углекислый газ. Этот процесс называется спиртовым брожением.
Энергии, накопленной при гликолизе, слишком мало для организмов, использующих кислород для своего дыхания. Вот почему в мышцах животных, в том числе и у человека, при больших нагрузках и нехватке кислорода образуется молочная кислота (С3Н6O3), которая накапливается в виде лактата. Появляется боль в мышцах. У нетренированных людей это происходит быстрее, чем у людей тренированных.
Третий этап – кислородный, состоящий из двух последовательных процессов – цикла Кребса, названного по имени Нобелевского лауреата Ганса Кребса, и окислительного фосфорилирования. Его смысл заключается в том, что при кислородном дыхании пируват окисляется до окончательных продуктов – углекислого газа и воды, а энергия, выделяющаяся при окислении, запасается в виде 36 молекул АТФ. (34 молекулы в цикле Кребса и 2 молекулы в ходе окислительного фосфорилирования). Эта энергия распада органических соединений обеспечивает реакции их синтеза в пластическом обмене. Кислородный этап возник после накопления в атмосфере достаточного количества молекулярного кислорода и появления аэробных организмов.
https://youtube.com/watch?v=M1QOYJrSQG4
Цикл Кребса представляет фазу III высвобождения энергии из продуктов питания. Каждый оборот этого цикла инициируется образованием цитрата с шестью атомами углерода из оксалоацетата (с четырьмя атомами углерода) и ацетилкофермента А; последующие реакции приводят к превращению оксалоацетата и образованию двух молекул углекислого газа. Атомы углерода, которые входят в образование углекислого газа, больше не доступны для клетки. В сопутствующее ступенчатые окисления, в которых атомы водорода или электроны удаляются из промежуточных соединений. Образующиеся во время цикла и через систему носителей, в конечном итоге, переносятся в кислород с образованием воды — количественно являются наиболее важным средством генерирования АТФ из АДФ и неорганического фосфата. Эти события известны как терминальное дыхание и окислительное фосфорилирование.
Окислительное фосфорилирование, или клеточное дыхание происходит на внутренних мембранах митохондрий, в которые встроены молекулы-переносчики электронов. В ходе этой стадии освобождается большая часть метаболической энергии. Молекулы-переносчики транспортируют электроны к молекулярному кислороду. Часть энергии рассеивается в виде тепла, а часть расходуется на образование АТФ.
Суммарная реакция энергетического обмена:
Образование
Формирование молекулы происходит в митохондриях и хлоропластах. Основополагающий момент в молекулярном синтезе кислоты – диссимиляционный процесс. Диссимиляция – процесс перехода сложного соединения до относительно простого за счет разрушения.
В рамках синтеза кислоты принято выделять несколько стадий:
- Подготовительная. Основа расщепления – пищеварительный процесс, обеспечивается за счет ферментативного действия. Распаду подвергается пища, попавшая в организм. Происходит жировое разложение до жирных кислот и глицерина. Белки распадаются до аминокислот, крахмал – до образования глюкозы. Этап сопровождается выделением энергии теплового характера.
- Бескислородная, или гликолиз. В основе лежит процесс распада. Происходит глюкозное расщепление с участием ферментов, при этом 60% выделяемой энергии превращается в тепло, остальная часть остается в составе молекулы.
- Кислородная, или гидролиз; Осуществляется внутри митохондрий. Происходит с помощью кислорода и ферментов. Участвует выдыхаемый организмом кислород. Завершается полной диссимиляцией. Подразумевает энергетическое выделение для формирования молекулы.
Существуют следующие пути молекулярного образования:
- Фосфорилирование субстратного характера. Основано на энергии веществ в результате окисления. Превалирующая часть молекулы формируется в митохондриях на мембранах. Осуществляется без участия ферментов мембраны. Совершается в цитоплазматической части посредством гликолиза. Допускается вариант образования за счет транспортировки фосфатной группы с иных макроэргических соединений.
- Фосфорилирование окислительного характера. Происходит за счет окислительной реакции.
- Фотофосфорилирование у растений в ходе фотосинтеза.
Фармакологические свойства АТФ
Благодаря оригинальной структуре молекула аденозинтрифосфата имеет характерное только для нее фармакологическое действие, не присущее никакому более из химических компонентов. АТФ нормализует концентрацию ионов магния и калия, при этом снижает концентрацию мочевой кислоты. За счет стимулирования энергетического обмена он улучшает:
- Активность ионотранспортных систем мембран клеток;
- Показатели липидного состава мембран;
- Антиоксидантную защитную систему миокарда;
- Активность мембранозависимых ферментов.
Благодаря нормализации метаболических процессов в миокарде, обусловленных гипоксией и ишемией, АТФ оказывает антиаритмическое, мембраностабилизирующее и противоишемическое действие.
Также этот препарат улучшает:
- Сократительную способность миокарда;
- Функциональное состояние левого желудочка;
- Показатели периферической и центральной гемодинамики;
- Коронарное кровообращение;
- Сердечный выброс (благодаря чему повышается физическая работоспособность).
В условиях ишемии роль АТФ – уменьшение потребления миокардом кислорода, активация функционального состояния сердца, в результате чего уменьшается одышка во время физической активности и сокращается частота приступов стенокардии.
У пациентов с суправентрикулярной и пароксизмальной наджелудочковой тахикардией, у больных с мерцанием и трепетанием предсердий данный препарат восстанавливает синусовый ритм и уменьшается активность эктопических очагов.
Модель синтеза АТФ: механический катализ
В 60—70 годах XX века Пол Бойер предположил, что синтез АТФ связан с изменениями конфигурации АТФ-синтазы, вызываемыми вращением γ-субъединицы, так называемый механизм изменения участка связывания («перевёртыш», англ. flip-flop). Исследовательской группе под руководством Джона Э. Уокера, относившейся тогда к Лаборатории молекулярной биологии в Кембридже, удалось выделить АТФ-синтазный каталитический комплекс F1 в кристаллической форме. На тот момент это была самая крупная из известных науке асимметричная белковая структура. Её исследования показали, что модель вращающегося катализа, предложенная Бойером, соответствует действительности. За это открытие Бойер и Уокер получили половину Нобелевской премии по химии в 1997 году. Вторую половину получил Йенс Кристиан Скоу «за первое открытие фермента, осуществляющего транспорт ионов — Na+,K+-аденозинтрифосфатазы».
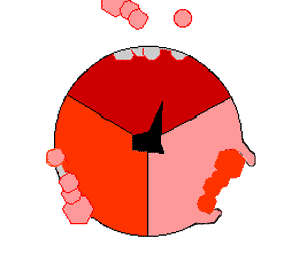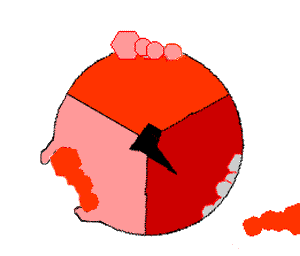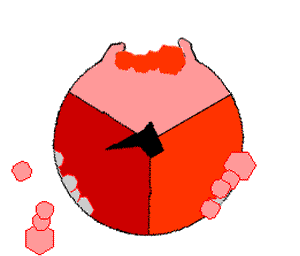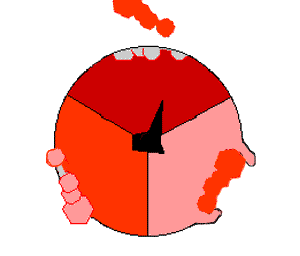
Механизм действия АТФ-синтазы. АТФ показан красным, АДФ и фосфат — розовым, вращающаяся субъединица γ — черным.
Кристалл F1 состоит из перемежающихся α- и β-субъединиц (по 3 каждого вида), расположенных как дольки апельсина вокруг асимметричной γ-субъединицы.
В соответствии с принятой моделью синтеза АТФ (также называемой моделью непостоянного катализа), градиент электрического поля, направленный поперёк внутренней митохондриальной мембраны и обусловленный электронной транспортной цепочкой, заставляет протоны проходить сквозь мембрану через АТФ-синтазный компонент FO.
Часть компонента FO (кольцо из c-субъединиц) вращается, когда протоны проходят через мембрану. Это c-кольцо жёстко связано с асимметричной центральной ножкой (состоящей в основном из γ-субъединицы), которая в свою очередь вращается внутри α3β3-участка компонента F1. Это приводит к тому, что три участка катализа, связывающиеся с нуклеотидами, претерпевают изменения в конфигурации, приводящие к синтезу АТФ.
Основные субъединицы (α3β3) компонента F1 соединены дополнительной боковой ножкой с неподвижным участком FO, что предотвращает их вращение вместе с γ-субъединицей.
Структура неповрёжденной АТФ-синтазы с низкой точностью выявлена при помощи электронной криомикроскопии (ЭКМ). Показано, что боковая ножка — это гибкая перемычка, похожая на канат, наматывающаяся на комплекс во время его работы.
При каждом обороте γ-субъединицы на 360 синтезируются три молекулы АТФ, При этом, видимо, у разных организмов из межмембранного пространства в матрикс проходит от 10 до 14 протонов — по числу с-субъединиц.
В определённых условиях каталитическая реакция может протекать в обратном направлении, при этом гидролиз АТФ вызывает прокачку протонов через мембрану.
В механизме изменения участка связывания задействован активный участок β-субъединицы, последовательно проходящий через три состояния.
В «открытом» состоянии АДФ и фосфат подходят к активному участку. Затем белок охватывает эти молекулы и свободно связывается с ними («свободное» состояние). Следующее изменение формы белка прижимает молекулы друг к другу («тесное» состояние), что приводит к формированию АТФ. Наконец, активный участок снова переходит в «открытое» состояние, освобождает АТФ и связывает следующую молекулу АДФ и фосфата, после чего цикл производства АТФ повторяется.
функции
АТФ играет незаменимую роль в энергетическом обмене практически всех живых организмов. По этой причине его часто называют энергетической валютой, поскольку его можно постоянно тратить и пополнять всего за несколько минут..
Прямой или косвенный, АТФ обеспечивает энергию для сотен процессов, в дополнение к действию в качестве донора фосфата.
В общем, АТФ действует как сигнальная молекула в процессах, происходящих внутри клетки, необходимо синтезировать компоненты ДНК и РНК и для синтеза других биомолекул участвует в трафике через мембраны, среди других.
Использование АТФ можно разделить на основные категории: транспорт молекул через биологические мембраны, синтез различных соединений и, наконец, механическая работа..
Функции СПС очень широки. Кроме того, он вовлечен в так много реакций, что было бы невозможно назвать их всех. Поэтому мы обсудим три конкретных примера, иллюстрирующих каждое из трех упомянутых применений..
Энергоснабжение для транспорта натрия и калия через мембрану
Ячейка является чрезвычайно динамичной средой, которая требует поддержания определенных концентраций. Большинство молекул не попадают в клетку случайно или случайно. Для того чтобы молекула или вещество могли проникнуть внутрь, оно должно делать это посредством своего конкретного переносчика..
Транспортеры — это белки, которые пересекают мембрану и функционируют как клеточные «привратники», контролирующие поток материалов. Следовательно, мембрана является полупроницаемой: она позволяет некоторым соединениям проникать, а другим — нет..
Одним из самых известных видов транспорта является натриево-калиевый насос. Этот механизм классифицируется как активный транспорт, так как движение ионов происходит против их концентрации, и единственный способ выполнить это движение — ввести энергию в систему в форме АТФ..
Подсчитано, что одна треть АТФ, образующегося в клетке, используется для поддержания работы насоса. Ионы натрия постоянно перекачиваются на поверхность клетки, а ионы калия — наоборот.
Логично, что использование АТФ не ограничивается транспортировкой натрия и калия. Есть другие ионы, такие как кальций, магний и другие, которые нуждаются в этой энергетической валюте, чтобы войти.
Участие в синтезе белка
Молекулы белка образованы аминокислотами, связанными между собой пептидными связями. Для их формирования требуется разрыв четырех высокоэнергетических связей. Другими словами, для образования белка средней длины необходимо гидролизовать значительное количество молекул АТФ..
Синтез белков происходит в структурах, называемых рибосомами. Они способны интерпретировать код, которым обладает РНК-мессенджер, и транслировать его в аминокислотную последовательность, АТФ-зависимый процесс.
В наиболее активных клетках синтез белка может направлять до 75% АТФ, синтезированного в этой важной работе. С другой стороны, клетка не только синтезирует белки, она также нуждается в липидах, холестерине и других необходимых веществах, и для этого требуется энергия, содержащаяся в связях АТФ.
С другой стороны, клетка не только синтезирует белки, она также нуждается в липидах, холестерине и других необходимых веществах, и для этого требуется энергия, содержащаяся в связях АТФ..
Обеспечить энергию для передвижения
Механическая работа является одной из важнейших функций СПС. Например, чтобы наше тело могло выполнять сокращение мышечных волокон, необходимо наличие большого количества энергии..
В мышцах химическая энергия может быть преобразована в механическую энергию благодаря реорганизации протеинов с сокращающей способностью, которые ее формируют. Длина этих структур изменена, укорочена, что создает напряжение, которое приводит к генерации движения.
У других организмов движение клеток также происходит благодаря наличию АТФ. Например, движение ресничек и жгутиков, которое позволяет перемещать определенные одноклеточные организмы, происходит посредством использования АТФ.
Другое конкретное движение — амебное, которое включает в себя выпячивание псевдоподы на концах клетки. Несколько типов клеток используют этот механизм локомоции, включая лейкоциты и фибробласты.
В случае половых клеток локомоция необходима для эффективного развития эмбриона. Эмбриональные клетки перемещаются на значительные расстояния от места их происхождения до региона, в котором они должны создавать специфические структуры..
Структура и номенклатура
Имеющаяся в митохондриях АТФ-синтаза F1FO очень хорошо исследована.
- компонент FO — трасмембранный домен,
- компонент F1 находится вне мембраны, в матриксе.
АТФ-синтазный комплекс FOF1 по форме напоминает плодовое тело гриба, у которого компонент F1 — это шляпка, ножка — это γ-субъединица компонента F1, а «корни» гриба — компонент FO, заякоренный в мембране.
В структурно-функциональном плане АТФ-синтетаза состоит из двух крупных фрагментов, обозначаемых символами F1 и FO. Первый из них (фактор сопряжения F1) обращён в сторону матрикса митохондрии и заметно выступает из мембраны в виде сферического образования высотой 8 нм и шириной 10 нм. Он состоит из девяти субъединиц, представленных пятью типами белков. Полипептидные цепи трёх субъединиц α и стольких же субъединиц β уложены в похожие по строению белковые глобулы, которые вместе образуют гексамер (αβ)3, имеющий вид слегка приплюснутого шара. Подобно плотно уложенным долькам апельсина, последовательно расположенные субъединицы α и β образуют структуру, характеризующуюся осью симметрии третьего порядка с углом поворота 120°. В центре этого гексамера находится субъединица γ, которая образована двумя протяжёнными полипептидными цепями и напоминает слегка деформированный изогнутый стержень длиной около 9 нм. При этом нижняя часть субъединицы γ выступает из шара на 3 нм в сторону мембранного комплекса F. Также внутри гексамера находится минорная субъединица ε, связанная с γ. Последняя (девятая) субъединица обозначается символом δ и расположена на внешней стороне F1.
Мембранная часть АТФ-синтетазы, называемая фактором сопряжения FO, представляет собой гидрофобный белковый комплекс, пронизывающий мембрану насквозь и имеющий внутри себя два полуканала для прохождения протонов водорода (ядер протия). Всего в состав комплекса FO входит одна белковая субъединица типа а, две копии субъединицы b, а также от 9 до 12 копий мелкой субъединицы c. Субъединица а (молекулярная масса 20 кДа) полностью погружена в мембрану, где образует шесть пересекающих её α-спиральных участков. Субъединица b (молекулярная масса 30 кДа) содержит лишь один сравнительно короткий погружённый в мембрану α-спиральный участок, а остальная её часть заметно выступает из мембраны в сторону F1 и закрепляется за расположенную на её поверхности субъединицу δ. Каждая из 9-12 копий субъединицы c (молекулярная масса 6-11 кДа) представляет собой сравнительно небольшой белок из двух гидрофобных α-спиралей, соединённых друг с другом короткой гидрофильной петлёй, ориентированной в сторону F1, а все вместе образуют единый ансамбль, имеющий форму погружённого в мембрану цилиндра. Выступающая из комплекса F1 в сторону FO субъединица γ как раз и погружена внутрь этого цилиндра и достаточно прочно зацеплена за него.
Номенклатура фермента имеет традиционное происхождение, поэтому довольно непоследовательна.
Обозначение компонента F1 является сокращением от «Fraction 1» (часть 1), а символом FO (в индексе записана буква O, а не ноль) обозначался участок связывания олигомицина.
Некоторые субъединицы фермента имеют также буквенные обозначения:
- Греческие: α, β, γ, δ, ε
- Латинские: a, b, c, d, e, f, g, h
Другие — более сложные обозначения:
- F6 (от «Fraction 6»)
- OSCP — белок, чувствительный к олигомицину (от англ. the oligomycin sensitivity conferral protein),
- A6L (названный так по названию гена, кодирующего его в митохондриальном геноме)
- IF1 (фактор ингибирования 1),
Компонент F1 достаточно велик (диаметр его составляет 9 нм), чтобы быть видимым в трансмиссионный электронный микроскоп при негативном окрашивании.
Частичками F1 усеяна внутренняя митохондриальная мембрана. Изначально считалось, что они содержат весь дыхательный аппарат митохондрии. Однако после долгих экспериментов группа Эфраима Рекера (впервые выделившая компонент F1 в 1961) показала, что эти частички связаны с АТФазной активностью в том числе и в разделённых митохондриях, и в субмитохондриальных частицах, формирующихся при ультразвуковом воздействии на митохондрии. Множество дальнейших исследований в разных лабораториях подтвердили эту АТФазную активность.
Натрия аденозинтрифосфат
– трифосаденин (натрия аденозинтрифосфат) (triphosadenine)
Состав и форма выпуска препарата
Раствор для в/в введения бесцветный или слегка желтоватый, прозрачный.
* динатрия аденозинтрифосфата дигидрат в пересчете на аденозинтрифосфорную кислоту.
Вспомогательные вещества: натрия карбонат безводный – 4.4 мг, натрия гидрокарбонат – 8 мг, динатрия эдетата дигидрат – 0.2 мг, пропиленгликоль – 0.1 мг, вода д/и – до 1 мл.
1 мл – ампулы (5) – пачки картонные.1 мл – ампулы (10) – пачки картонные.1 мл – ампулы (5) – упаковки ячейковые контурные из пленки поливинилхлоридной (1) – пачки картонные.1 мл – ампулы (5) – упаковки ячейковые контурные из пленки поливинилхлоридной (2) – пачки картонные.
1 мл – ампулы (5) – упаковки ячейковые контурные из пленки поливинилхлоридной (4) – пачки картонные (для стационаров).1 мл – ампулы (5) – упаковки ячейковые контурные из пленки поливинилхлоридной (5) – пачки картонные (для стационаров).
1 мл – ампулы (5) – упаковки ячейковые контурные из пленки поливинилхлоридной (10) – пачки картонные (для стационаров).1 мл – ампулы (5) – упаковки ячейковые контурные из пленки поливинилхлоридной (50) – пачки картонные (для стационаров).
1 мл – ампулы (5) – упаковки ячейковые контурные из пленки поливинилхлоридной (100) – пачки картонные (для стационаров).
Фармакологическое действие
Средство, улучшающее метаболизм и энергообеспечение тканей. АТФ является естественным компонентом тканей организма – участвует во многих процессах обмена веществ. При распаде АТФ на АДФ и неорганический фосфат высвобождается энергия, необходимая для мышечного сокращения и различных биохимических процессов.
АТФ участвует в передаче возбуждения в адренергических и холинергических синапсах, облегчает передачу возбуждения с блуждающего нерва на сердце. По-видимому, АТФ – один из медиаторов, возбуждающих аденозиновые рецепторы.
Усиливает мозговое и коронарное кровообращение, способствует увеличению периферического кровообращения.
Трифосаденин – производное аденозина. Аденозин является агонистом пуринергических рецепторов, активация которых приводит к угнетению деполяризации процессов проведения электрических импульсов в синусовом и AV-узлах. Этот эффект лежит в основе антиаритмического действия трифосаденина при наджелудочковых тахикардиях. Действует кратковременно в течение нескольких секунд.
Фармакокинетика
После парентерального введения проникает в клетки органов, где расщепляется на аденозин и неорганический фосфат с высвобождением энергии. В дальнейшем продукты распада включаются в ресинтез АТФ.
Острый инфаркт миокарда, тяжелая артериальная гипотензия, тяжелая брадикардия, СССУ, AV-блокада II-III степени (за исключением пациентов с искусственным водителем ритма), острая и хроническая сердечная недостаточность в стадии декомпенсации, ХОБЛ, бронхиальная астма, синдром удлиненного интервала QT, беременность, период грудного вскармливания, возраст до 18 лет, повышенная чувствительность к трифосаденину.
С осторожностью
Брадикардия, AV-блокада I степени, блокада ножек пучка Гиса, фибрилляция и трепетание предсердий, аретриальная гипотензия, ИБС, гиповолемия, перикардит, стеноз клапанов сердца, артериовенозный шунт “слева-направо”, недостаточность мозгового кровообращения, состояния после пересадки сердца (менее 1 года).
Дозировка
Вводят в/в. Дозу устанавливают индивидуально, в зависимости от показаний.
При в/м введении: возможны головная боль, тахикардия, увеличение диуреза, гиперурикемия.
При в/в введении: возможны тошнота, гиперемия кожи лица, головная боль, слабость.
Аллергические реакции: редко – зуд, гиперемия кожи.
Лекарственное взаимодействие
При одновременном применении с сердечными гликозидами повышается риск развития побочных эффектов (в т.ч. аритмогенного действия).
Применение в пожилом возрасте
С осторожностью применять у пациентов пожилого возраста. Описание препарата Натрия аденозинтрифосфат основано на официально утвержденной инструкции по применению и утверждено компанией–производителем
Описание препарата Натрия аденозинтрифосфат основано на официально утвержденной инструкции по применению и утверждено компанией–производителем.
Обнаружили ошибку? Выделите ее и нажмите Ctrl+Enter.
Разница между АТФ и НАДФН
Определение
АТФ относится к фосфорилированному нуклеотиду, состоящему из аденозина и трех фосфатных групп, обеспечивая энергию для многих биохимических клеточных процессов путем ферментативного гидролиза, особенно для АДФ. Напротив, НАДФН относится к кофактору, который используется для пожертвования электронов и водородов в реакции, катализируемые некоторыми ферментами. Таким образом, эти определения содержат основное различие между АТФ и НАДФН.
Химическая формула
Химическая формула АТФ является C10ЧАС16N5О13п3 в то время как химическая формула NADPH является C21ЧАС29N7О17п3.
Роль
Другое различие между ATP и NADPH состоит в том, что ATP является энергетической валютой ячейки, в то время как NAPDH является основной восстанавливающей способностью ячейки.
Синтез
Путь синтеза способствует еще одному различию между АТФ и НАДФН. Клеточное дыхание, фотофосфорилирование и ферментация являются путями, которые продуцируют АТФ, в то время как пентозофосфатный путь у животных и легкая реакция фотосинтеза у растений являются путями, которые продуцируют НАДФН.
использование
АТФ обеспечивает энергию для различных типов биохимических реакций, включая анаболические реакции, деление клеток и движение, в то время как NADPH обеспечивает электроны и протоны для темновой реакции фотосинтеза и многих биосинтетических и окислительно-восстановительных реакций у животных. Следовательно, это еще одно различие между АТФ и НАДФН.
Заключение
АТФ является основной энергетической валютой клетки. Его гидролиз высвобождает энергию, необходимую для большинства биохимических реакций внутри клетки. С другой стороны, НАДФН является основной восстанавливающей силой клетки. Он обеспечивает как электроны, так и атомы водорода для биохимических реакций. Самое главное, НАДФН является кофактором. Таким образом, основное различие между АТФ и НАДФН заключается в их роли внутри клетки.
АТФ мышц
Что такое АТФ?
АТФ (аденозинтрифосфат, аденозинтрифосфорная кислота) – основное макроэргическое соединение организма. Состоит из аденина (азотистого основания), рибозы (углевод) и трех последовательно расположенных фосфатных остатков, причем второй и третий фосфатные остатки присоединяются макроэргической связью. Структура АТФ выглядит следующим образом (рис.1).
Рис. 1. Структура АТФ
История открытия АТФ
АТФ был открыт(а) в 1929 году немецким биохимиком Карлом Ломаном (Karl Lohmann) и, независимо Сайрусом Фиске (Cyrus Fiske) и Йеллапрагада Субба Рао (Yellapragada Subba Rao) из Гарвардской медицинской школы. Однако структура АТФ была установлена только спустя несколько лет. Владимир Александрович Энгельгардт в 1935 году показал, что для сокращения мышц необходимо присутствие АТФ. В 1939 году В. А. Энгельгардт совместно со своей женой М. Н. Любимовой предъявили доказательства, что миозин проявляет ферментную активность при этом расщепляется АТФ и высвобождается энергия. Фриц Альберт Липманн (Fritz Albert Lipmann) в 1941 году показал, что АТФ является основным переносчиком энергии в клетке. Ему принадлежит фраза «богатые энергией фосфатные связи». В 1948 году Александр Тодд (Alexander Todd) (Великобритания) синтезировал АТФ. В 1997 году Пол Д. Бойер (Paul D. Boyer) и Джон Э. Уокер (John E. Walker) получили Нобелевскую премию по химии за разъяснение ферментативного механизма, лежащего в основе синтеза АТФ.
Содержание АТФ в мышечных волокнах
Количество АТФ в тканях организма человека относительно невелико, поскольку он (она) в тканях не запасается. В мышечных волокнах содержится 5 ммоль на кг сырой ткани или 25 ммоль на кг сухой мышечной ткани.
Реакция гидролиза
Непосредственным источником энергии при мышечной деятельности является АТФ, который (ая) находится в саркоплазме мышечных волокон. Освобождение энергии происходит в результате реакции гидролиза АТФ.
Гидролиз АТФ – реакция, протекающая в мышечных волокнах, при которой АТФ, взаимодействуя с водой распадается на АДФ и фосфорную кислоту. При этом выделяется энергия. Гидролиз АТФ ускоряется ферментом АТФ-азой. Этот фермент находится на каждой миозиновой головке толстого филамента.
Реакция гидролиза АТФ имеет следующий вид:
АТФ+Н2О→АДФ+Н3РО4 + энергия
В результате гидролиза 1 моль АТФ выделяется энергия, равная 42-50 кДж (10-12 ккал). Скорость протекания реакции гидролиза повышают ионы кальция. Следует отметить, что АДФ (аденозиндифосфат) в мышечных волокнах выполняет роль универсального акцептора (приёмника) высокоэнергетического фосфата и используется для образования АТФ.
Фермент АТФ-аза
Фермент АТФ-аза расположен на миозиновых головках, что играет существенную роль в сокращении мышечных волокон. Активность фермента АТФ-азы лежит в основе классификации мышечных волокон на медленные (I тип), промежуточные (IIA тип) и быстрые (IIB тип).
Химическая энергия, выделяемая в результате гидролиза в мышечных волокнах, расходуется на: сокращение мышечных волокон (взаимодействие белков актина и миозина) и на их расслабление (работу кальциевого и натрий-калиевого насосов). При взаимодействии с актином одна молекула миозина за одну секунду гидролизует 10 молекул АТФ.
Запасы АТФ в мышечных волокнах невелики и могут обеспечить выполнение интенсивной работы в течение 1-2 с. Дальнейшая мышечная деятельность осуществляется благодаря быстрому восстановлению (ресинтезу) АТФ, поэтому при сокращении мышечных волокон в них одновременно протекают два процесса: гидролиз АТФ, дающий необходимую энергию и ресинтез АТФ, восполняющий запасы АТФ в мышечных волокнах.
Ресинтез АТФ
Ресинтез АТФ – синтез АТФ в мышечных волокнах из различных энергетических субстратов во время физической работы. Его формула выглядит следующим образом:
АДФ+фосфат+энергия → АТФ
Ресинтез АТФ может осуществляться двумя путями:
- без участия кислорода (анаэробный путь);
- с участием кислорода (аэробный путь).
Если в саркоплазме мышечных волокон недостаточно АТФ, то затрудняется процесс их расслабления. Возникают судороги.
Более подробно строение и функции мышц описаны в моих книгах «Гипертрофия скелетных мышц человека» и «Биомеханика мышц»
Литература
- Михайлов С.С. Спортивная биохимия. – М.: Советский спорт, 2009.– 348 с.
- Волков Н.И., Несен Э.Н., Осипенко А.А., Корсун С.Н. Биохимия мышечной деятельности.- Киев: Олимпийская литература, 2000.- 504 с.
Макроэргические соединения – химические соединения, содержащие связи, при гидролизе которых происходит освобождение значительного количества энергии.
Сущность понятия
 Перед изучением понятия АТФ необходима его расшифровка. Данный термин означает нуклеозидтрифосфат, который существенно значим для энергетического и вещественного обмена в составе организма.
Перед изучением понятия АТФ необходима его расшифровка. Данный термин означает нуклеозидтрифосфат, который существенно значим для энергетического и вещественного обмена в составе организма.
Это уникальный энергетический источник, лежащий в основе биохимических процессов. Данное соединение является основополагающим для ферментативного образования.
АТФ был открыт в Гарварде в 1929 году. Основоположниками стали ученые Гарвардской медицинской школы. В их число вошли Карл Ломан, Сайрус Фиске и Йеллапрагада Суббарао. Они выявили соединение, которое по строению напоминало адениловый нуклеотид рибонуклеиновых кислот.
Отличительной особенностью соединения было содержание трех остатков фосфорной кислоты вместо одного. В 1941 году ученый Фриц Липман доказал, что АТФ имеет энергетический потенциал в пределах клетки. Впоследствии был обнаружен ключевой фермент, который получил название АТФ-синтаза. Его задача – образование в митохондриях кислотных молекул.
АТФ – это энергетический аккумулятор в клеточной биологии, является обязательным для успешного осуществления биохимических реакций.
 Биология аденозинтрифосфорной кислоты предполагает ее образование в результате энергетического обмена. Процесс состоит из создания 2 молекул на второй стадии. Остальные 36 молекул появляются на третьем этапе.
Биология аденозинтрифосфорной кислоты предполагает ее образование в результате энергетического обмена. Процесс состоит из создания 2 молекул на второй стадии. Остальные 36 молекул появляются на третьем этапе.
Скопление энергии в структуре кислоты происходит в связующей части между остатками фосфора. В случае отсоединения 1 фосфорного остатка происходит энергетическое выделение 40 кДж.
В результате кислота превращается в аденозиндифосфат (АДФ). Последующее фосфатное отсоединение способствует появлению аденозинмонофосфата (АМФ).
Следует отметить, цикл растений предусматривает повторное использование АМФ и АДФ, в результате которого происходит восстановление этих соединений до состояния кислоты. Это обеспечивается процессом фотосинтеза.