Реакции цикла кребса
Содержание:
Химизм
На конечном этапе цикла ключевой фермент цикла АТФ-цитратлиаза разрушает цитрат на оксалоацетат и ацетил-CoA, используя энергию одной АТФ. Далее происходят следующие реакции:
- Ацетил~CoA + CO2 + ФдH2 → Пируват + Фд
- Пируват + АТФ → ФЕП + АДФ + Фн
- ФЕП + АТФ + 2H+ → глицеральдегид-3-фосфат + АМФ + ФФн
Полученный глицеральдегид-3-фосфат используется для синтеза материалов клетки. Общее уравнение ассимиляции имеет вид:
- 3CO2 + 2ФдH2 + 2НАДФН·H+ + ФАДH2 + НАДН·Н+ + 5АТФ→ глицеральдегид-3-фосфат
Ассимиляция углекислого газа идёт с большой затратой АТФ и восстановительных эквивалентов. В целом цикл считается анаэробным, поскольку включает много ферментов и восстановителей (Fe4S4 бактериальных ферредоксинов), которые чувствительны к кислороду (из аэробных бактерий такой цикл обнаружен только у Hydrogenobacter).
Этот цикл является возможным кандидатом в реакции, которые могли протекать на Земле в добиологических условиях, и, по этой причине, изучение этого цикла представляет интерес для понимания происхождения жизни. Принципиально, что данный цикл является автокаталитическим — в нём, в отличие от окислительного ЦТК в результате одного оборота цикла количество реагентов, в том числе акцепторов СО2, увеличивается, а не уменьшается, как в цикле Кребса. Так же, было доказано, что некоторые из реакций можно катализировать, используя обычные минералы, в частности пять реакций протекает в присутствии ZnS (сфалерит) на свету.
Химизм
На конечном этапе цикла ключевой фермент цикла АТФ-цитратлиаза разрушает цитрат на оксалоацетат и ацетил-CoA, используя энергию одной АТФ. Далее происходят следующие реакции:
- Ацетил~CoA + CO2 + ФдH2 → Пируват + Фд
- Пируват + АТФ → ФЕП + АДФ + Фн
- ФЕП + АТФ + 2H+ → глицеральдегид-3-фосфат + АМФ + ФФн
Полученный глицеральдегид-3-фосфат используется для синтеза материалов клетки. Общее уравнение ассимиляции имеет вид:
- 3CO2 + 2ФдH2 + 2НАДФН·H+ + ФАДH2 + НАДН·Н+ + 5АТФ→ глицеральдегид-3-фосфат
Ассимиляция углекислого газа идёт с большой затратой АТФ и восстановительных эквивалентов. В целом цикл считается анаэробным, поскольку включает много ферментов и восстановителей (Fe4S4 бактериальных ферредоксинов), которые чувствительны к кислороду (из аэробных бактерий такой цикл обнаружен только у Hydrogenobacter).
Этот цикл является возможным кандидатом в реакции, которые могли протекать на Земле в добиологических условиях, и, по этой причине, изучение этого цикла представляет интерес для понимания происхождения жизни. Принципиально, что данный цикл является автокаталитическим — в нём, в отличие от окислительного ЦТК в результате одного оборота цикла количество реагентов, в том числе акцепторов СО2, увеличивается, а не уменьшается, как в цикле Кребса. Так же, было доказано, что некоторые из реакций можно катализировать, используя обычные минералы, в частности пять реакций протекает в присутствии ZnS (сфалерит) на свету.
ГЛАВА 15. ПЕНТОЗОФОСФАТНЫЙ ПУТЬ И ГЛЮКОНЕОГЕНЕЗ
Пируват-карбоксилаза — митохондриальный фермент, тогда как другие ферменты глюконеогенеза находятся в цитоплазме. Оксалоацетат, продукт пируват-карбоксилазной реакции, переносится через митохондриальную мембрану в форме малата. Его восстановление в малат происходит в митохондриях под действием NADH-зависимой малат-дегидрогеназы. Образующийся при этом малат транспортируется переносчиком через митохондриальную мембрану и вновь окисляется в оксалоацетат NAD+-зависимой малат-дегидрогеназой цитозоля.
Оксалоацетат подвергается в цитозоле одновременно декарбоксилироваиию и фосфорилированию под действием фосфоенол- пируват-карбоксикиназы.
На этой стадии происходит отделение СО2, присоединившегося к пирувату под действием прируват-карбоксилазы. Реакция фосфорилирования становится энергетически возможной благодаря одновременному декарбоксилироваиию. Процессы де- карбоксилирорания часто приводят в движение реакции, которые в ином случае были бы высокоэндергоническими. Мы вновь встретимся с этим механизмом в разделе, посвященном синтезу жирных кислот.
Стехиометрия глюконеогенеза описывается уравнением
2 Пируват + 4 АТР + 2GTP+ 2NADH+ 2Н2О → Глюкоза + 4ADP+ 2GDP+ 6 Рi + 2NAD+
∆G = — 9 ккал/моль.
Стехиометрия обращения гликолиза носит иной характер:
2 Пируват + 2АТР + 2NADH + 2Н2O →Глюкоза + 2АDР + 2Рi+ 2NAD+
∆G = + 20 ккал/моль.
Заметим, что для синтеза глюкозы из пирувата путем глюконеогенеза используется шесть высокоэнергетических фосфатных связей, тогда как в процессе превращения глюкозы в пируват при гликолизе образуются только две молекулы АТР. Таким образом, избыточная «цена» глюконеогенеза равна четырем высокоэнергетическим фосфатным связям в расчете на одну молекулу глюкозы, синтезируемой из пирувата. Для превращения энергетически неблагоприятного процесса (обращение гликолиза, ∆G’ = + 20 ккал/моль) в энергетически благопрятный (глюконеогенез, ∆G = — 9 ккал/моль) требуются четыре лишние высокоэнергетические фосфатные связи. Рассматривая это энергетическое различие между гликолизом и глюконеогенезом под другим углом зрения, напомним, что вклад одного эквивалента АТР изменяет константу равновесия реакции примерно в 108 раз (разд. 11.7). Следовательно, вклад четырех дополнительных высокоэнергетических связей при глюконеогенезе изменяет эту константу в 1032 раз, что делает превращение пирувата в глюкозу термодинамически выгодным.
Рис. 15.6. Молекулярная модель карбоксибиотина
15.19. Глюконеогенез и гликолиз регулируются реципрокно
Глюконеогенез и гликолиз координируются таким образом, что, когда активность одного из этих путей находится на относительно низком уровне, другой путь является высокоактивным. В случае одновременной высокой активности обеих последовательностей реакций происходил бы гидролиз четырех ~ Р (два АТР + два GTP) на каждый цикл реакции. В условиях, существующих в клетке, и гликолиз, и глюконеогенез представляют собою высокоэкзергонические процессы, так что термодинамических барьеров для осуществления таких циклов нет. Тот факт, что активность этих двух процессов никогда не достигает высокого уровня одновременно, обусловливается скорее всего соответствующей регуляцией отдельных ферментов каждого процесса. Например, АМР стимулирует фосфофруктокиназу (разд. 12.9), но ингибирует фруктозо-1,6-бисфосфатазу. Цитрат оказывает на эти ферменты противоположное действие. Следовательно, фосфорилирование фруктозо-6- фосфата, этап, лимитирующий скорость гликолиза, усиливается при низком энергетическом заряде клетки. Напротив, при высоком энергетическом заряде и избытке промежуточных продуктов цикла трикарбоновых кислот происходит гидролиз фруктозо-1 ,6-бисфосфата и стимулируется глюконеогенез. Пируваткиназа (разд. 12.7) и пируват-карбоксилаза (разд. 15.16) также регулируются реципрокно. Фруктозо-1,6- бисфосфат стимулирует, а АТР ингибирует пируваткиназу, тогда как пируват-карбоксилаза стимулируется ацетил-СоА и подавляется ADP. Таким образом, обогащение клеток печени топливными молекулами и АТР благоприятствует превращению пирувата в фосфоенолпируват и глюконеогенезу.
Нарушения активности пируватдегидрогеназы[править | править код]
Недостаточность тиаминаправить | править код
В нервной ткани ведущую роль в синтезе АТФ играют гликолиз и дальнейший синтез ацетил-КоА в пируватдегидрогеназной реакции, который затем окисляется в цикле Кребса. Для нормального функционирования пируватдегидрогеназы необходим тиамин. При недостаточности тиамина активность фермента снижается, и нервная ткань испытывает недостаток в производимой энергии. Развиваются гиперлактатемия, заболевания нервной системы; в тяжелых случаях — болезнь Вернике, психоз Корсакова. Недостаточность тиамина наблюдается при хроническом алкоголизме, из-за плохого питания.
(Запомните, что, хотя ацетил-КоА может образовываться из жирных кислот независимо от пируватдегидрогеназной реакции, головной мозг не может использовать жирные кислоты в качестве источника энергии, поскольку они не проходят через гематоэнцефалический барьер.)
Пируватдегидрогеназный мульферментный комплекс
Суммарное уравнение отражает окислительное декарбоксилирование пирувата, восстановление НАД до НАДН и образование ацетил-SKoA.
Суммарное уравнение окисления пировиноградной кислоты
Превращение состоит из пяти последовательных реакций, осуществляется мультиферментным комплексом, прикрепленным к внутренней митохондриальной мембране со стороны матрикса. В составе комплекса насчитывают 3 фермента и 5 коферментов:
- Пируватдегидрогеназа (Е1, ПВК-дегидрогеназа), ее коферментом является тиаминдифосфат (ТДФ), катализирует 1-ю реакцию.
- Дигидролипоат-ацетилтрансфераза (Е2), ее коферментом является липоевая кислота, катализирует 2-ю и 3-ю реакции.
- Дигидролипоат-дегидрогеназа (Е3), кофермент – ФАД, катализирует 4-ю и 5-ю реакции.
Помимо указанных коферментов, которые прочно связаны с соответствующими ферментами, в работе комплекса принимают участие коэнзим А и НАД.
Суть первых трех реакций сводится к декарбоксилированию пирувата (катализируется пируватдегидрогеназой, Е1), окислению полученного гидроксиэтила до ацетила и переносу ацетила на коэнзим А (катализируется дигидролипоат-ацетилтрансферазой, Е2).
Реакции синтеза ацетил-SКоА
Оставшиеся 2 реакции необходимы для возвращения липоевой кислоты и ФАД в окисленное состояние (катализируются дигидролипоат-дегидрогеназой, Е3). При этом образуется НАДН.
Реакции образования НАДН
Регуляция пируватдегидрогеназного комплекса
Регулируемым ферментом ПВК-дегидрогеназного комплекса является первый фермент – пируватдегидрогеназа (Е1). Два вспомогательных фермента – киназа и фосфатаза обеспечивают регуляцию активности пируватдегидрогеназы путем ее фосфорилирования и дефосфорилирования.
Вспомогательный фермент киназа активируется при избытке конечного продукта биологического окисления АТФ и продуктов ПВК-дегидрогеназного комплекса – НАДН и ацетил-S-КоА. Активная киназа фосфорилирует пируватдегидрогеназу, инактивируя ее, в результате первая реакция процесса останавливается.
Фермент фосфатаза, активируясь ионами кальция или инсулином, отщепляет фосфат и активирует пируватдегидрогеназу.
Регуляция активности пируватдегидрогеназы
Таким образом, работа пируватдегидрогеназы подавляется при избытке в митохондрии (в клетке) ацетил-SКоА и НАДН, что позволяет снизить окисление пирувата и, следовательно, глюкозы в случае когда энергии достаточно.
Если АТФ мало или имеется влияние инсулина, то образуется ацетил-SКоА. Последний в зависимости от условий будет направляться либо в цикл трикарбоновых кислот с образованием энергии АТФ, либо на синтез холестерина и жирных кислот.
Ферменты
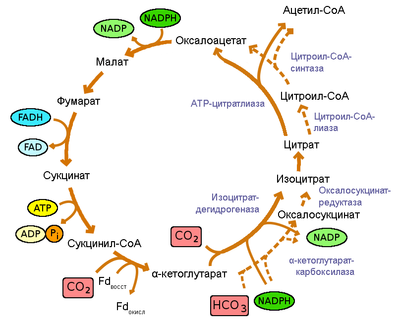
Цикл Арнона. Пунктиром обозначены альтернативные пути реакции.
Считается, что три реакции цикла Кребса необратимы, а значит, в цикле Арнона эти реакции должны осуществляться другими ферментами, чтобы сделать цикл обратимым: так, сукцинатдегидрогеназа заменена на фумаратредуктазу, НАД+-зависимая α-кетоглутаратдегидрогеназа на ферредоксин-зависимую α-кетоглутаратсинтазу, а цитратсинтаза на АТФ-цитратлиазу. Эти три фермента обычно считаются характерными для данного цикла.
Большинство бактерий, которые используют этот цикл — мезофилы, однако представители филума Aquificae растут при температуре 70 °C и выше (Aquifex aeolicus вплоть до 95 °C). При таких условия термически неустойчивый распадается на сукцинат и коэнзим А, что сопровождается потерей энергии и делает невозможным его дальнейшее использование в цикле. Aquificae (как было показано на ) решают эту проблему, тратя дополнительный АТФ на превращение α-кетоглутарата в изоцитрат совместным действием биотин-зависимой α-кетоглутараткарбоксилазы и недекарбоксилирующей изоцитратдегидрогеназы, что делает процесс необратимым при повышенной температуре.
У некоторых видов основной путь цикла может иметь некоторые отличия. Так вместо АТФ-цитратлиазы расщепление цитрата могут осуществлять два других фермента: цитрил-CoA синтаза и . Однако, оба эти фермента филогенетически близки к АТФ-цитратлиазе. Их обнаружили у представителей Aquificaceae (но не у других Aquificae). Более того, некоторые протеобактерии (например, Magnetococcus sp. штамм MC-1), вероятно, обладают новым типом АТФ-цитратлиазы.
Метаболизм
Одно из важнейших свойств живого (вспоминаем биологию) — это обмен веществ с окружающей средой. Действительно, только живое существо может что-то поглощать из окружающей среды, и что-то потом в неё выделять.
В биохимии обмен веществ принято называть «метаболизм». Обмен веществ, обмен энергией с окружающей средой — это метаболизм.
Когда мы, допустим, съели бутерброд с курицей, мы получили белки (курица) и углеводы (хлеб). В процессе пищеварения белки распадутся до аминокислот, а углеводы — до моносахаров. То, что я описал сейчас, называется катаболизм, то есть распад сложных веществ на более простые. Первая часть метаболизма — это катаболизм.
Ещё один пример. Ткани в нашем организме постоянно обновляются. Когда отмирает старая ткань, её обломки растаскивают макрофаги, и они заменяется новой тканью. Новая ткань создаётся в процессе синтеза белка из аминокислот. Синтез белка происходит в рибосомах. Создание нового белка (сложного вещества) из аминокислот (простого вещества) — это анаболизм.
Итак, анаболизм — это противоположность катаболизму. Катаболизм — это разрушение веществ, анаболизм — это создание веществ. Кстати, чтобы их не путать, запомните ассоциацию: «Анаболики. Кровью и потом». Это голливудский фильм (довольно скучный, на мой взгляд) о спортсменах, применяющих анаболики для роста мышц. Анаболики — рост, синтез. Катаболизм — обратный процесс.
Клеточное дыхание
Для нормальной жизнедеятельности живым клеткам постоянно требуется энергия. Ее главный универсальный источник — аденозинтрифосфат (АТФ), способный встраиваться в белки организма напрямую. Это соединение получается в результате ряда реакций окисления, носящих общее название «клеточное дыхание». При этом происходит постепенный распад органических веществ вплоть до простейших неорганических — углекислого газа CO2 и воды H2O.
Структурное строение молекул АТФ содержит фосфорангидридные связи, которые имеют свойство накапливать высвобожденную при прохождении реакций клеточного дыхания энергию, поэтому называются макроэргическими. Так создаются энергетические запасы клеток, которые могут высвобождается при необходимости разрывом этих связей. Процесс синтеза АТФ и класса вспомогательных соединений включает три этапа:
Гликолиз происходит в цитоплазме.
В матриксе митохондрий проходят все химические реакции цикла Кребса.
Окислительное фосфорилирование на внутренней мембране митохондрий.
Преобразование аденозиндифосфата (АДФ) в АТФ характерно для всех этапов. Но наибольшее суммарное количество молекул с макроэргическими связями образуется при фосфорилировании. Это не значит, что процессы гликолиза и ЦК менее важны. Многие соединения, образующиеся во время их протекания, участвуют в регуляции клеточного дыхания.
Липидный обмен
Если во время приема пищи в печень поступает избыток глюкозы, который не используется для синтеза гликогена и других синтезов, то она превращается в липиды – холестерол и триацилглицеролы. Поскольку запасать ТАГ печень не может, то их удаление происходит при помощи (ЛПОНП). Холестерол используется, в первую очередь, для синтеза желчных кислот, также он включается в состав липопротеинов низкой плотности (ЛПНП) и ЛПОНП.
При определенных условиях – голодание, длительная мышечная нагрузка, сахарный диабет I типа, богатая жирами диета – в печени активируется синтез кетоновых тел, используемых большинством тканей как альтернативный источник энергии.
БИОХИМИЯ — Л. Страйер — 1984
ГЛАВА 15. ПЕНТОЗОФОСФАТНЫЙ ПУТЬ И ГЛЮКОНЕОГЕНЕЗ
Пируват-карбоксилаза — митохондриальный фермент, тогда как другие ферменты глюконеогенеза находятся в цитоплазме. Оксалоацетат, продукт пируват-карбоксилазной реакции, переносится через митохондриальную мембрану в форме малата. Его восстановление в малат происходит в митохондриях под действием NADH-зависимой малат-дегидрогеназы. Образующийся при этом малат транспортируется переносчиком через митохондриальную мембрану и вновь окисляется в оксалоацетат NAD+-зависимой малат-дегидрогеназой цитозоля.
Оксалоацетат подвергается в цитозоле одновременно декарбоксилироваиию и фосфорилированию под действием фосфоенол- пируват-карбоксикиназы.
На этой стадии происходит отделение СО2, присоединившегося к пирувату под действием прируват-карбоксилазы. Реакция фосфорилирования становится энергетически возможной благодаря одновременному декарбоксилироваиию. Процессы де- карбоксилирорания часто приводят в движение реакции, которые в ином случае были бы высокоэндергоническими. Мы вновь встретимся с этим механизмом в разделе, посвященном синтезу жирных кислот.
Стехиометрия глюконеогенеза описывается уравнением
2 Пируват + 4 АТР + 2GTP+ 2NADH+ 2Н2О → Глюкоза + 4ADP+ 2GDP+ 6 Рi + 2NAD+
∆G = — 9 ккал/моль.
Стехиометрия обращения гликолиза носит иной характер:
2 Пируват + 2АТР + 2NADH + 2Н2O →Глюкоза + 2АDР + 2Рi+ 2NAD+
∆G = + 20 ккал/моль.
Заметим, что для синтеза глюкозы из пирувата путем глюконеогенеза используется шесть высокоэнергетических фосфатных связей, тогда как в процессе превращения глюкозы в пируват при гликолизе образуются только две молекулы АТР. Таким образом, избыточная «цена» глюконеогенеза равна четырем высокоэнергетическим фосфатным связям в расчете на одну молекулу глюкозы, синтезируемой из пирувата. Для превращения энергетически неблагоприятного процесса (обращение гликолиза, ∆G’ = + 20 ккал/моль) в энергетически благопрятный (глюконеогенез, ∆G = — 9 ккал/моль) требуются четыре лишние высокоэнергетические фосфатные связи. Рассматривая это энергетическое различие между гликолизом и глюконеогенезом под другим углом зрения, напомним, что вклад одного эквивалента АТР изменяет константу равновесия реакции примерно в 108 раз (разд. 11.7). Следовательно, вклад четырех дополнительных высокоэнергетических связей при глюконеогенезе изменяет эту константу в 1032 раз, что делает превращение пирувата в глюкозу термодинамически выгодным.
Рис. 15.6. Молекулярная модель карбоксибиотина
15.19. Глюконеогенез и гликолиз регулируются реципрокно
Глюконеогенез и гликолиз координируются таким образом, что, когда активность одного из этих путей находится на относительно низком уровне, другой путь является высокоактивным. В случае одновременной высокой активности обеих последовательностей реакций происходил бы гидролиз четырех ~ Р (два АТР + два GTP) на каждый цикл реакции. В условиях, существующих в клетке, и гликолиз, и глюконеогенез представляют собою высокоэкзергонические процессы, так что термодинамических барьеров для осуществления таких циклов нет. Тот факт, что активность этих двух процессов никогда не достигает высокого уровня одновременно, обусловливается скорее всего соответствующей регуляцией отдельных ферментов каждого процесса. Например, АМР стимулирует фосфофруктокиназу (разд. 12.9), но ингибирует фруктозо-1,6-бисфосфатазу. Цитрат оказывает на эти ферменты противоположное действие. Следовательно, фосфорилирование фруктозо-6- фосфата, этап, лимитирующий скорость гликолиза, усиливается при низком энергетическом заряде клетки. Напротив, при высоком энергетическом заряде и избытке промежуточных продуктов цикла трикарбоновых кислот происходит гидролиз фруктозо-1 ,6-бисфосфата и стимулируется глюконеогенез. Пируваткиназа (разд. 12.7) и пируват-карбоксилаза (разд. 15.16) также регулируются реципрокно. Фруктозо-1,6- бисфосфат стимулирует, а АТР ингибирует пируваткиназу, тогда как пируват-карбоксилаза стимулируется ацетил-СоА и подавляется ADP. Таким образом, обогащение клеток печени топливными молекулами и АТР благоприятствует превращению пирувата в фосфоенолпируват и глюконеогенезу.
ПредыдущаяСледующая
Ферменты
Цикл Арнона. Пунктиром обозначены альтернативные пути реакции.
Считается, что три реакции цикла Кребса необратимы, а значит, в цикле Арнона эти реакции должны осуществляться другими ферментами, чтобы сделать цикл обратимым: так, сукцинатдегидрогеназа заменена на фумаратредуктазу, НАД+-зависимая α-кетоглутаратдегидрогеназа на ферредоксин-зависимую α-кетоглутаратсинтазу, а цитратсинтаза на АТФ-цитратлиазу. Эти три фермента обычно считаются характерными для данного цикла.
Большинство бактерий, которые используют этот цикл — мезофилы, однако представители филума Aquificae растут при температуре 70 °C и выше (Aquifex aeolicus вплоть до 95 °C). При таких условия термически неустойчивый распадается на сукцинат и коэнзим А, что сопровождается потерей энергии и делает невозможным его дальнейшее использование в цикле. Aquificae (как было показано на ) решают эту проблему, тратя дополнительный АТФ на превращение α-кетоглутарата в изоцитрат совместным действием биотин-зависимой α-кетоглутараткарбоксилазы и недекарбоксилирующей изоцитратдегидрогеназы, что делает процесс необратимым при повышенной температуре.
У некоторых видов основной путь цикла может иметь некоторые отличия. Так вместо АТФ-цитратлиазы расщепление цитрата могут осуществлять два других фермента: цитрил-CoA синтаза и . Однако, оба эти фермента филогенетически близки к АТФ-цитратлиазе. Их обнаружили у представителей Aquificaceae (но не у других Aquificae). Более того, некоторые протеобактерии (например, Magnetococcus sp. штамм MC-1), вероятно, обладают новым типом АТФ-цитратлиазы.
История изучения
Биологическая роль некоторых реакций цикла Кребса (ЦК) была изучена американским биохимиком венгерского происхождения Альбертом Сент-Дьердьи. В частности, он выделил ключевой компонент ЦТК — фумарат. Исследования в этом направлении продолжил Ганс Кребс. В итоге он установил всю последовательность реакций и соединений, образующиеся на всех этапах процесса. Ученый не смог определить, с преобразования какой кислоты начинается цикл — лимонной или изолимонной. Сейчас известно, что это лимонная кислота. Поэтому ЦК называют также цитратным или циклом лимонной кислоты.
Про понятие «Цикл Кребса» простыми словами
Метаболизм
Метаболизм – это энергетический обмен, происходящий в нашем организме. Мы вдыхаем кислород и выдыхаем углекислый газ. Только живое существо может что-то брать из окружающей среды и обратно возвращать в другом виде.
Допустим, мы решили позавтракать и съели хлеб с курицей. Хлеб — это углеводы, курица – это белки.
В течении этого времени переваренные углеводы распадутся до моносахаридов, а белки до аминокислот.
Это начальная стадия – катаболизм. На этой ступени по своему строению сложные распадаются на более простые.
Также, в качестве примера можно привести обновление поверхности кожи. Они постоянно меняются. Когда верхний слой кожи отмирает, макрофаги убирают омертвевшие клетки и появляется новая ткань. Она создается путем сбора белка из органических соединений. Это протекает в рибосомах. Совокупность действий возникновения сложного состава (белка) из простого (аминокислот) называется анаболизмом.

Анаболизм:
- рост,
- увеличение,
- расширение.
Катаболизм:
- расщепления,
- деление,
- уменьшения.
Название можно запомнить, просмотрев фильм «Анаболики». Там идет речь о спортсменах, применяющих анаболические препараты для роста и увеличения мышечной массы.
Что такое Цикл Кребса?
В 30 годы 20 века ученый Ганс Кребс занимается изучение мочевины. Затем он переселяется в Англию и приходит к такому выводу, что некоторые ферменты катализируются в нашем теле. За это ему вручили Нобелевскую премию.
Мы получаем энергию благодаря глюкозе, содержащейся в эритроцитах. Действию перехода декстроза в энергию помогают митохондрии. Затем конечный продукт превращается в аденозинтрифосфат или АТФ. Именно АТФ является главной ценностью организма. Получаемое вещество насыщает энергией и органы нашего тела. Сама по себе глюкоза не может видоизмениться в АТФ, для этого нужны сложные механизмы. Этот переход и называется Циклом Кребса.
Цикл Кребса — это постоянные химические превращения, происходящие внутри каждого живого существа. Так оно называется, так как процедура повторяется без остановки
В итоге этого явления мы приобретаем аденозинтрифосфорную кислоту, которая считается жизненно важной для нас
Важным условием является дыхание клетки. Во время прохождения всех стадий обязательно должен присутствовать кислород. На данном этапе также происходит создание новых аминокислот и углеводов. Эти элементы играют роль строителей организма, можно сказать это явление выполняет еще одну значительную роль — строительную. Для эффективности этих функций нужны и другие микро и макроэлементы и витамины. При недостатке хоть одного элемента, работа органов нарушается.
Этапы цикла Кребса
Здесь происходит деление одной молекулы глюкозы на две части пировиноградной кислоты. Она является важным звеном в процессе обмена веществ и от нее зависит работа печени. Она имеется во многих фруктах и ягодах. Ее часто используют в косметических целях. В результате еще может появиться молочная кислота. Она содержится в клетках крови, мозга, мышц. Затем мы получим кофермент А. Его функция — перенос углерода в разные части тела. При присоединении с оксалатом получаем цитрат. Кофермент А полностью распадается, также получаем молекулу воды.
На втором вода отделяется от цитрата. В итоге появляется акатиновое соединение, она поможет при получении изоцитрата. Так, например, мы можем узнать качество фруктов и соков, нектаров. Образуется NADH — оно необходимо при окислительных процессах и обмене веществ.
Происходит процесс соединения с водой, и высвобождается энергия аденозинтрифосфата. Получение оксалоцетата. Функционирует в митохондриях.
По каким причинам замедляется энергетический обмен?
Наше тело имеет особенность адаптироваться к еде, к жидкости и тому, сколько мы двигаемся. Эти вещи сильно влияют на метаболизм.
Еще в те далекие времена человечество выживало в тяжелых погодных условиях при болезнях, голоде, неурожае. Сейчас медицина двинулась вперед, поэтому в развитых странах люди стали дольше жить и лучше зарабатывать, не прикладывая всех своих сил. В наши дни люди чаще употребляют мучные, сладкие кондитерские изделия и мало двигаются. Такой образ жизни ведет к замедлению работы элементов.
Чтобы этого не было, в первую очередь необходимо включить в рацион цитрусовые. В них содержится комплекс витаминов и других важных веществ. Большую роль играет лимонная кислота, содержащаяся в ее составе. Она играет роль в химическом взаимодействии всех ферментов и названа в честь Цикла Кребса.